Conținut în limba
- Titlul complet al proiectului; Susținerea și transferul magnetizării nucleilor hiperpolarizați
- Acronimul; PN-III-P4-ID-PCE-2016-0887
- Rezumatul proiectului
- Rezultatele obținute în fiecare etapă de derulare a proiectului
- Rezultatele finale ale proiectului
PLAN DE REALIZARE A PROIECTULUI
Informația RMN se bazează pe cantitatea de magnetizare utilizată și modul în care această magnetizare colectivă este conservată în timpul experimentului. Recent, s-au înregistrat progrese semnificative în polarizarea unui număr mare de spini nucleare folosind ca sursa radicali liberi, prin procedura cunoscută sub numele de Polarizare Dinamică Nucleară (DNP). Aceasta procedură este o revoluție pentru RMN, o spectroscopie care era cunoscută pentru lipsa de sensibilitate, deoarece poate multiplica raportul semnal-zgomot până la 10’000 ori.
Dezvoltarea de aplicații ale acestei tehnici foarte recente rămâne o provocare, în special din cauza problemelor legate de duratele de viață ale magnetizării ‘hiperpolarizate’. Transmiterea magnetizării în locația dorită in moleculă, către site-ul de interacțiune într-o celulă, sau site-ul de imagistică destinat in interiorul corpului depinde în mod critic de durata de viață a acestei magnetizări. Ameliorări ale timpului de viață pot fi proiectate chiar și într-un context RMN standard, prin optimizarea de sonde moleculare și tehnici de excitație, înainte de punerea în aplicare într-un context DNP. Metodele RMN propuse în acest proiect trebuie să contribuie în mod decisiv la transformarea DNP-RMN in starea lichidă într-o tehnică mai versatilă. Noi modalități de conservare a magnetizării sunt propuse. Stări optime de spin pentru a conserva magnetizarea în molecule cu mai multe nuclee magnetice cuplate vor fi evaluate teoretic și testate experimental. Magnetizarea cu durate lungi de viată poate călători pe distanțe lungi, aproape neschimbată – prin urmare, sensibilitatea de detecție. De aceea, transformări și interacțiuni ale moleculelor endogene mici si ale proteinelor complexe pot fi urmărite cu mai mare ușurința prin RMN. Aceasta poate duce la numeroase aplicații: de la studii ale mecanismului și dinamicii interacțiunilor biomoleculare, până la angiografia prin rezonanță magnetică folosind sonde moleculare endogene.
- Obiectivele generale si rezultatele estimate a fi obtinute;
| Obiectivele generale | Rezultatele estimate a fi obținute |
| Etapa 1 – Crearea unei strategii adaptate pentru susținerea magnetizării în moleculele alese;Act. 1.1. Stabilirea de modele pentru transferul polarizării în moleculele propuse. | Modele pentru transferul magnetizării. |
| Etapa 2 – Caracterizarea moleculelor, transferul oprim al polarizării, utilizând cuplaje J;Act. 2.1. Controlul transferului de polarizare în moleculele propuse. | Verificarea modelelor, rezultate privind transferul prin spațiu a magnetizării. |
| Etapa 3 – Dezvoltarea unei metode 2D pentru NMR hiperpolarizat. Validare, publicare și diseminare a Rezultatelor. | Spectroscopie 2D hiperpolarizata. Publicare și diseminare. |
- Institutia coordonatoare, eventual cu sigla institutiei si datele de contact; Nu este cazul
- Componenta consortiului; Nu este cazul
- Autoritatea contractanta (finantatoare a proiectului); UEFISCDI
- Durata proiectului; 12.07.2017 – 31.12.2019
- Activitatile si responsabilitatile aferente fiecarui participant (planul de realizare);
- Bugetul proiectului – defalcat finantare de la bugetul de stat si cofinantare;
| Nr.crt | Categorii de cheltuieli | 2017 | 2018 | 2019 | Total |
| 1 | Cheltuieli de personal | 127170 | 281586 | 269244 | 678000 |
| 2 | Cheltuieli de logistica | 45620 | 42630 | 6750 | 95000 |
| 3 | Cheltuieli de deplasari | 4500 | 6750 | 10750 | 22000 |
| 4 | Cheltuieli indirecte | 44322 | 76753 | 65925 | 187000 |
| 5 | TOTAL(1+2+3+4) | 221612 | 407719 | 352669 | 982000 |
4. Rezultatele obținute în fiecare etapă de derulare a proiectului (raport public, indicatori de rezultat, etc.)
Etapa 1
În această perioadă a proiectului s-au realizat următoarele pentru îndeplinirea obiectivelor propuse:
- S-a creat o strategie adaptată pentru susținerea magnetizării în moleculele continand un ciclu aromatic adiacent nucleelor de azot.
- S-au stabilit modele pentru studiul transferului polarizării pentru substanțele achiziționate: monometil fumarat, dimetil fumarat, citrat, piruvat, lactat, Ala-Gly, citrulină, oxalat, acid fumaric, glicina, glutamină, acid glutamic, acid aspartic, asparagină. Pentru același tip de experimente au fost cumpărate și o serie de compuși marcați: glicina 1-13C, glucoză 6-13C și asparagină 4-13
Descrierea pe larg a experimentelor efectuate și prezentarea rezultatelor:
Metoda LLS (Long-lived states) a fost utilizată pentru prima dată pentru a demonstra interacțiile dintre molecule și ionii metalici diamagnetici. Această metodă poate fi folosită în două contexte: (i) în experimente RMN hiperpolarizate folosind d-DNP (dissolution Dynamic Nuclear Polarization), pentru îmbunătățirea sensibilității: în aceste experimente LLS este utilizat pentru menținerea magnetizării hiperpolarizate; (ii) în experimente RMN care pornesc de la o magnetizare în care avem echilibru termic la codificarea LLS. În acest context informația oferită de metoda LLS poate fi complementară datelor obținute din relaxarea longitudinală standard.
Derivații de oxodiazol utilizați în acest studiu au substituenți diferiți de o parte și alta a inelului oxodiazolic. În acest studiu s-a putut observa interacția dintre atomii donor precum atomii de azot din moleculele organice și ionii metalici prin metoda LLS.
Experimentele RMN au fost înregistrate la un câmp magnetic de NMR B0 =11.75 T folosind spectrometrul Bruker Avance care operează la o frecvență de 500.13 MHz. Temperatura utilizată pentru experimente a fost de 250C; spectrele au fost prelucrate cu ajutorul programelor Topspin, Mestrec și datele experimentale procesate cu Matlab.
Curbele de relaxare au fost fitate folosind o funcție a programului Matlab specifică iar erorile au fost calculate dintr-o analiza Monte-Carlo.
Detecția directă a semnalelor de 15N a fost realizată utilizând standardul de formaldehidă marcată în 15N (număr scani – 8192 tranzienți și recovery delay de 15 s ). Pentru înregistrarea spectrelor de proton și a experimentelor LLS au fost utilizați următorii parametri: număr de scani – 64 tranzienți și recovery delay de 20 s. Experimentele T1 au fost înregistrate utilizând 16 tranzienți și recovery delay de 25 s.
Spectrele RMN de 1H și 15N înregistrate pentru molecula de oxodiazol studiată sunt prezentate în Figura 1.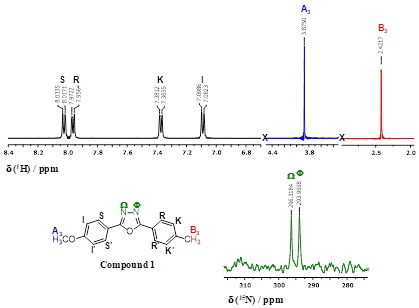
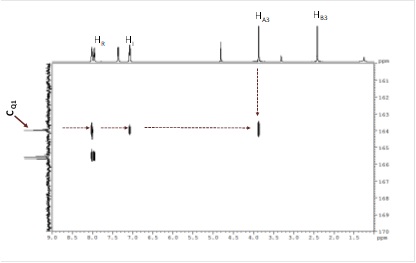
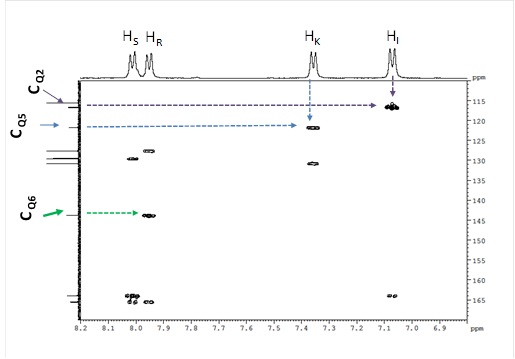
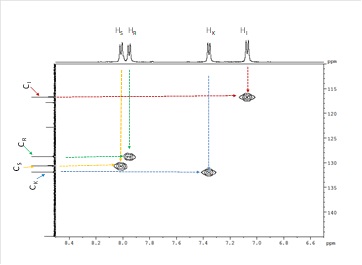
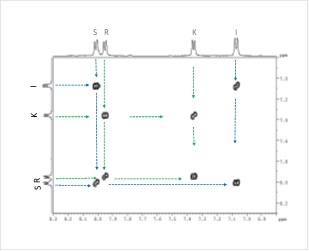
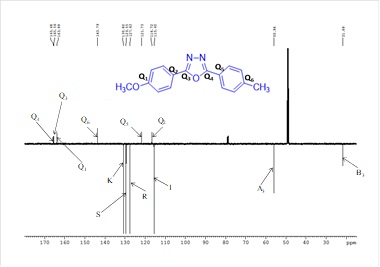
Caracterizarea structurală a oxodiazolului s-a realizat prin înregistrarea spectrelor 1D și 2D-RMN (Figurile 2A-2G).
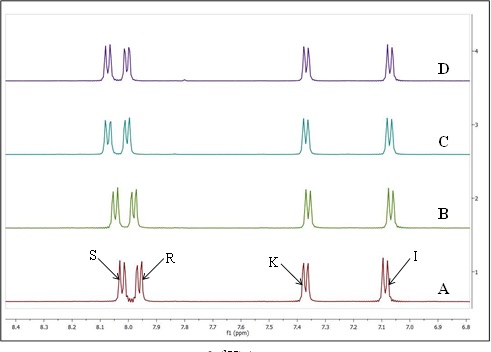
1H-NMR (500.13 MHz, MeOD-d4, δ ppm, J Hz): 8.02 (d, 2H, H-S, H-S’, 8.5 Hz), 7.96 (d, 2H, H-R, H-R’, 8.0 Hz), 7.37 (d, 2H, H-K, H-K’, 8.0 Hz), 7.09 (d, 2H, H-I, H-I’, 8.5 Hz), 3.87 (s, 3H, A3), 2.41 (s, 3H, H-B3).
13C-NMR (125.77 MHz, MeOD-d4, δ ppm): 165.7 (CQ4), 165.6 (CQ3), 164.0 (CQ1), 143.8 (CQ6), 130.8 (C-K, C-K’), 129.67 (C-S, C-S’), 127.6 (C-R, C-R’), 121.7 (CQ5), 116.7 (CQ2), 115.6 (C-I, C-I’), 55.9 (C-A3), 21.7 (C-B3).
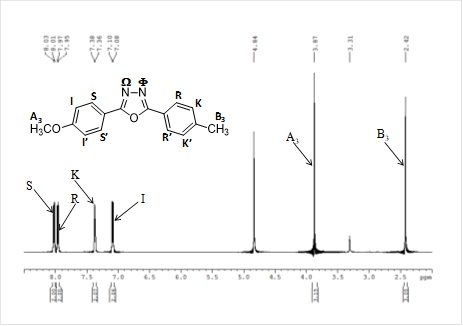
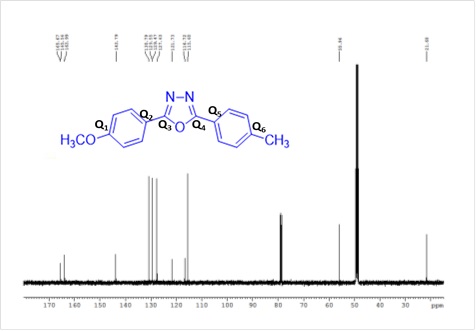
A fost creată o strategie pentru studierea interacțiilor dintre compusul organic (oxodiazol) și ionii metalici (argint Ag(I)) utilizând metoda LLS s-a preparat o soluție stock de CF3SO3Ag. Cote parte din aceasta soluție au fost adăugate în tubul RMN peste soluția de oxodiazol (Figura 3).
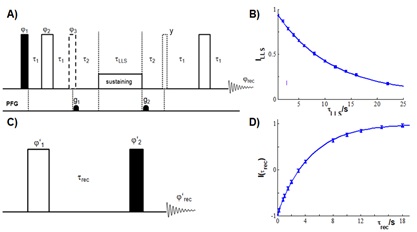
Metoda LLS a relevat o constantă de relaxare până la TLLS = 1/RLLS ~ 10 secunde pentru protonii aromatici din ciclul aromatic. Secvența de pulsuri utilizată pentru excitarea și detecția LLS este prezentată în Figura 4.
În Tabelul 1 sunt prezentate constantele de relaxare longitudinale ale derivaților de oxadiazol.
Table 1. Valorile R1 și RLLS pentru martor și pentru amestecurile oxodiazol- soluție Ag(I) (echivalenți molar de la 0.25 până la 0.75 echivalenți molari).
| R1 (s-1) | RLLS (s-1)Semnale detectate pentru spinul R și spinul I
(și semnale detectate pe spinul K și spinul S) |
|||||||
| Eq. de Ag(I) | 0 | 0.25 | 0.5 | 0.75 | 0 | 0.25 | 0.5 | 0.75 |
| Spin R | 0.22±0.01 | 0.27±0.01 | 0.30±0.01 | 0.31±0.01 | 0.096±0.005 | 0.139±0.005 | 0.152±0.004 | 0.166±0.005 |
| Spin K | 0.29±0.01 | 0.36±0.01 | 0.40±0.01 | 0.41±0.01 | (0.094±0.005) | (0.138±0.005) | (0.153±0.005) | (0.162±0.006) |
| Spin I | 0.33±0.01 | 0.40±0.01 | 0.43±0.02 | 0.45±0.01 | 0.122±0.004 | 0.172±0.008 | 0.179±0.008 | 0.204±0.012 |
| Spin S | 0.22±0.01 | 0.27±0.01 | 0.30±0.01 | 0.32±0.01 | (0.110±0.010) | (0.150±0.020) | (0.171±0.008) | (0.180±0.016) |
Constantele de timp ale relaxării longitudinale, T1=1/R1, sunt semnificativ mai scurte decât timpii de viata LLS. Degazarea probelor mărește toate constantele de relaxare cu un factor de 2. Constanta R1 măsurată pentru oxadiazol în prezența ionilor de argint crește cu 0.05-0.07 s-1 (cca. 20%) față de proba în care s-au adăugat 0.25 echivalenți molari de sare de argint și rămâne aproximativ aceeași la concentrații mai mari de argint. În ceea ce privește LLS, adăugarea de argint (I) la soluția de oxadiazol conduce la o creștere cu 70% a constantelor de relaxare RLLS pentru perechea de spini (I, S) și cu 65% pentru perechea de spini (S, K). Variațiile în RLLS = 1 / TLLS la adăugarea de argint oferă îmbunătățiri semnificative în comparație cu variațiile în R1 = 1 / T1, ceea ce face ca LLS să fie o metodă sensibilă pentru cartografierea interacțiunii (Figura 5 și Figura 6).
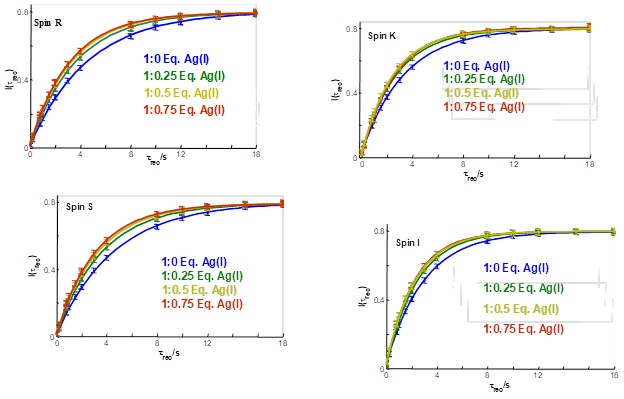
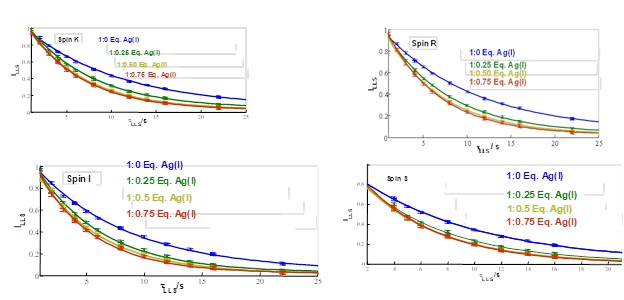
Interacțiilor dintre derivații de oxodiazol și ionii de argint (I) au fost detectate utilizând experimentele LLS de proton. Constantele de relaxare al LLS excitate asupra nucleilor de hidrogen situați în imediata vecinătate a atomilor donori par să fie mult mai sensibile decât relaxarea longitudinala RMN standard pentru interacții.
Hiperpolarizarea spinilor nucleari detectați poate oferi perspective suplimentare asupra acestui tip de interacții la probe având concentrații scăzute.
Rezultatele experimentale obținute în aceasta etapă au fost diseminate prin publicare unui articol în Journal of Magnetic Resonance (FI = 2.432):
Cristina Stavarache, Anamaria Hanganu, Anca Paun, Codruta Paraschivescu, Mihaela Matache, Paul R. Vasos, “Long-lived states detect interactions between small molecules and diamagnetic metal ions”, Journal of Magnetic Resonance, 2017, 284, 15-19, http://dx.doi.org/10.1016/j.jmr.2017.09.001.
De asemenea rezultatele preliminare obținute au fost diseminate prin prezentări orale în cadrul următoarelor manifestări științifice de către membrii echipei de cercetare:
- Paul Vasos, “Enhanced NMR to follow enzymatic reactions in living cells”, Oral presentation, 20th Romanian International Conference on Chemistry and Chemical Engineering, 6-9 September 2017, Poiana Brasov, Romania.
- Aude Sadet, CRUK Cambridge Institute, Workshop, 6-9 december 2017, “Molecular probes useful for in vivo MRI experiments“
- Descrierea/prezentarea diferitelor evenimente derulate in cadrul proiectului (exp: conferinte, seminarii, intalniri ale partenerilor, etc.);
- Paul Vasos, “Enhanced NMR to follow enzymatic reactions in living cells”, Oral presentation, 20th Romanian International Conference on Chemistry and Chemical Engineering, 6-9 September 2017, Poiana Brasov, Romania.
- Aude Sadet, CRUK Cambridge Institute, Workshop, 6-9 december 2017, “Molecular probes useful for in vivo MRI experiments“
- Aude Sadet, Glasgow, United Kingdom 25 – 27 June 2018, “Artificial Water Channels Faraday Discussion“
- Link-uri catre diverse alte pagini de interes pentru vizitator. Ex: pagini legislative din domeniul de activitate al proiectului, proiecte similare sau complementare, paginile web ale institutiilor partenere in proiect, etc;……………………………………
- Datele de contact ale directorului de proiect; Vasos Paul
mail: paul.vasos@icub.unibuc.ro
Telefon: 021.3159249
Rezultatele finale ale proiectului- nu este cazul
Cod Proiect PN-III-P4-ID-PCE-2016-0887
Competiție 2016
- Cristina Stavarache, Anamaria Hanganu, Anca Paun, Codruta Paraschivescu, Mihaela Matache, Paul R. Vasos, “Long-lived states detect interactions between small molecules and diamagnetic metal ions”, Journal of Magnetic Resonance, 2017, 284, 15-19, http://dx.doi.org/10.1016/j.jmr.2017.09.001.
https://www.ncbi.nlm.nih.gov/pubmed/28938134
- Viorel Vasile Nastasa, Cristina Stavarache, Anamaria Hanganu, Adina Coroaba, Alina Nicolescu, Calin Deleanu, Aude Sadet, Paul Vasos, “Hyperpolarised NMR to Follow Water Proton Transport through Membrane Channels via Exchange with Biomolecules”, Faraday Discussions, 2018, DOI: 10.1039/C8FD00021B.
Etapa 2
Caracterizarea moleculelor, transferul optim al polarizării utilizând cuplaje J; Controlul transferului de polarizare în moleculele propuse
Rezumatul rezultatelor obținute:
1) Demonstrarea transferului de polarizare dinspre protonii hiperpolarizați ai apei înspre molecule; discutarea vitezei de transfer in contextul interpunerii unei membrane lipidice în care se afla canale pe parcursul protonilor transferați (articol publicat in Faraday Discussions, 2018, 209, 67-82 2, DOI: 10.1039/c8fd00021b);
2) Demonstrarea efectelor cuplajului J intre protonii Ala-Gly asupra transferului de polarizare si a interacțiilor stărilor coerente cu viață lungă (Long Lived Coherences – LLC’s) cu magnetizarea apei – articol aflat in faza discuției cu referenți internaționali (rezultatele au contribuit pentru articolele: Sadet et al., JACS 2019, Sadet et al., Sci. Rep. 2019);
3) Ierarhizarea timpilor de viață ai magnetizării care pot fi atinși folosind metode de tip ‚Long-lived states’ (LLS) pentru diferite biomolecule cu potențial de utilizare ca biomarkeri pentru RMN in vivo (e.g., acid fumaric, asparagină, acid glutamic, citrulină – articol in curs de redactare);
4) Studiul transferului de magnetizare între forma redusa și forma oxidata a glutationului: experiențe în curs pentru a propune noi metode pentru monitorizarea stresului oxidant prin monitorizarea conversiei între forma redusa și forma oxidata via rezonantă magnetică.
Organizarea proiectului și comunicare științifică: Rezultatele obținute au fost comunicate într-o conferință științifică internațională organizata de UK Royal Society, the Faraday Discussions Meeting, Glasgow, June 2018, communication by Dr A. Sadet și publicate in Faraday Discussions (articol situat in zona maxima de influenta in domeniul chimie fizica, dupa scorul de influenta cotat in iunie 2018 de uefiscdi.ro); echipa proiectului a fost completata prin cooptarea unui student MSc care asigura avansul parții teoretice și de calcule a proiectului (Florin Teleanu); a fost efectuată o campanie experimentală de măsurători folosind hiperpolarizarea (dissolution – Dynamic Nuclear Polarisation) la Scola Normala din Paris, Laboratoire des Biomolecules și Universitatea din Viena; rezultatele sunt folosite în cadrul cursului susținut anual la Scoala Doctorala a Facultatii de Chimie, Universitatea din Bucuresti și acestea contribuind și la realizarea unui capitol de carte contractat și în curs de redactare pentru cartea editata de Royal Society of Chemistry: „Long-Lived Nuclear Spin Order”.
Rezultatele experimentale obținute în aceasta etapă au fost diseminate prin publicare unui articol în Faraday Discussions (FI = 3.427) “Hyperpolarised NMR to Follow Water Proton Transport through Membrane Channels via Exchange with Biomolecules”, Faraday Discussions, 2018, 209, 67-82, DOI: 10.1039/C8FD00021B.
Etapa 3
Dezvoltarea unei metode 2D pentru NMR hiperpolarizat. Validare, publicare si diseminare a Rezultatelor
Finalizarea activităților științifice, publicare și diseminare
Spectroscopia RMN bazata pe protoni poate fi utilizată în studiul plierii și a stabilirii conformațiilor în membrane a peptidelor și a proteinelor.
Cea mai simplă cale pentru obținerea informație structurale pentru peptide cu mase mai mici de 10 kDa este spectroscopia de corelație proton-proton (COSY).
În cele ce urmează vom descrie un experiment care permite caracterizarea “high-resolution” a conformațiilor peptidelor în mai puțin de 1 minut. Durata foarte scurtă a experimentelor descrise a fost obținută prin îmbunătățirea semnalelor folosind metoda D-DNP. Pentru a demonstra acest concept am ales să folosim dipeptida alanină-glicina (AlaGly) dizolvată în HDO hiperpolarizată – sistem model pentru studierea interacțiilor peptidă-lipozomi prin COSY hiperpolarizat (Figura 1).

Figura 1. (adaptat pentru lucrarea noastră Sadet et al., JACS 2019). Spectrul de proton al peptidei AlaGly obținut fără hiperpolarizare
Pentru a obține spectre COSY hiperpolarizate peptida AlaGly a fost dizolvată într-un amestec hiperpolarizat de 4% H2O în D2O, cu o îmbunătățire a protonilor HDO, εHDO, în intervalul 100-200. In spectrul DNP-enhanced 2D COSY, intensitățile semnalelor peptidei rezultate din HDO s-au îmbunătățit cu un factor ε = IHiperpolarizat/Iconvențional ≈ 405. În spectru 2D COSY hiperpolarizat (Figura 2), pe lângă încrucișarea semnalelor Gly-HN și Ala-HN rezultate prin magnetizarea transmisă prin cuplaje J intrareziduale la protonii Hα, s-a putut observa apariția mai multor semnale intersectate datorate îmbunătățirii intensității semnalului. Datorită sensibilității crescute a experimentului, se poate observa corelația Ala-HN și Ala-Hβ rezultată prin transferul prin cuplaje 4J; de asemenea, se pot deduce corelații inter-reziduale între protonii Gly-HN și Ala-Hα.

Figura 2. (adaptat pentru lucrarea noastră Sadet et al., JACS 2019)
(A) Corelațiile proton-proton în spectru 2D COSY hiperpolarizat în regiunea amidică a AlaGly și atribuirea semnalelor. Spectrul hiperpolarizat COSY înregistrat într-un minut (roșu) este suprapus cu un spectru COSY convențional obținut fără hiperpolarizare (albastru). Ambele spectre au fost procesate în același fel. Atribuirea semnalelor se bazează pe spectrul COSY convențional care cuprinde atât regiunea amidică cât și regiunea alifatică. (B) Suprapunerea proiecțiilor spectrelor de proton de corelație din spectrele COSY: hiperpolarizat (roșu) și convențional (albastru, amplificat cu un factor de 400).
Spectru 2D COSY convențional, la echilibru termic, a arătat doar transferul magnetizării de la Ala-HN la Ala-Hα și de la Gly-HN la Gly-Hα1 și Gly-Hα2. În Tabelul 1 colana II sunt prezentate îmbunătățirile de semnal obținute pentru diferitele poziții din spectrul 2D precum și semnalele noi detectate.
Tabelul 1. Îmbunătățirea intensității semnalului (S), ε = S (COSY hiperpolarizat) / S (COSY convențional), pentru încrucișarea picurilor selectate și raportul semnalului dintre intensitatea semnalului peptidei AlaGly libera (Sfp) și interacțiunea lipozomi-AlaGly (Sl-p), ρ = Sfp/ Sl-p, observate în spectrul 2D COSY hiperpolarizat
| Semnal | ε | ρ |
| Gly-HN/Gly-Hα | 114 | 6 |
| Ala-HN/Ala-Hα | 190 | 14 |
| Ala-HN/Ala-Hβ | doar în COSY hiperpolarizata | Niciun semnal în proba de lipozomi |
| Gly-HN/Ala-Hα | doar în COSY hiperpolarizata | Niciun semnal în proba de lipozomi |
| Gly-HN/HDO | Niciun semnal în proba de lipozomi | |
| Ala-HN/HDO | Niciun semnal in proba de lipozomi |
aDoar COSY hiperpolarizat inducă faptul ca în spectru COSY convențional nu s-au observat aceste corelări
Relaxarea longitudinală a magnetizării în timpul transferului probei între polarizator și sistemul de detecție este crucială pentru obținerea îmbunătățirii. Avantajul HDO hiperpolarizat este constanta sa de relaxare, care este suficient de mare, T1 (HDO) ≈ 8 s, ceea ce permite observarea magnetizării până la zeci de secunde după hiperpolarizare. Prin comparație, se așteaptă ca în urma polarizării directe a nucleilor 1H în AlaGly urmată de dizolvare, transfer și injecție să rezulte o îmbunătățire a semnalului mai scăzută, chiar și pentru protonii metilici ce au o cea mai scăzută relaxare, cu valori tipice T1 (1H) de ∼2 s în câmpuri magnetice înalte și chiar mai scăzute în timpul etapei de transfer în câmpuri joase. Prin urmare, se pot obține spectre multidimensionale hiperpolarizate în intervalul de timp ꞌimpusꞌ de relaxarea HDO, în loc să fie limitate de relaxarea mult mai rapidă a moleculei țintă. Aceste îmbunătățiri obținute ne-au permis creșterea amplitudinii semnalelor – foste corelații invizibile peste pragul de detecție (Tabelul 1).
Corelațiile proton-proton au fost detectate adecvat în spectru 2D COSY hiperpolarizat. Comparativ cu experimentul 2D COSY convențional, trebuie să luam în considerate următoarele aspecte:
- Pentru a păstra rezoluția a fost utilizată, în dimensiunea indirectă, o fereastră spectrală îngustă. Chiar și cu ferestre spectrale înguste, rezoluția în dimensiunea indirectă a experimentului hiperpolarizat rămâne o problemă din cauza timpului de evoluție limitat, t1max. Pentru a îmbunătăți rezoluția în aceste condiții, pot fi utile experimentele „SOFT-COSY” .
- Metoda poate fi împiedicată de rezonanțele foarte intense ale apei, ceea ce impune evitarea efectelor de amortizare de radiațiilor care pot distorsiona spectrele înregistrate; de asemenea, hiperpolarizarea HDO trebuie menținută. Prin urmare, se reduce dimensiunea directă a spectrelor (Figura 2) și se alege o rezonantă selectivă de excitare a peptidei.
- Experimentul nu necesită „recovery-delay” convențional (τrecovery=4s), întrucât polarizarea protonului este completată de schimbul magnetic cu solventul.
Am studiat interacțiunea AlaGly cu lipozomii (Figura 2). Lipozomii considerați au fost vezicule mari unilamelare (LUVs).

Figura 3. (adaptat pentru lucrarea noastră Sadet et al., JACS 2019)
Modificări ale spectrelor 2D COSY hiperpolarizate datorate interacțiunilor cu lipozomii. (A, B) COSY hiperpolarizat și proiecțiile acestora (integrale peste dimensiune indirectă) pentru AlaGly fără lipozomi (roșu) și în prezența lipozomilor (albastru, în proiecții scara este înmulțită cu un factor de 4). (C) Reprezentarea AlaGly libera și o conformație unde interacționează cu lipozomii. (D) Captura dintr-o traiectorie MD care arată faptul că peptida formează o legătură de hidrogen (linia galbenă) între reziduu Ala și dioleoilfosfatidilcolina (DOPC) pe suprafața bistratificată.
S-a observată o diferență foarte mare între spectrele înregistrate în prezența și în absența lipozomilor. În prezența lipozomilor s-a remarcat o scădere a intensității semnalului din zona amidică. Pierderea semnalului în spectrele înregistrate în prezența lipozomilor comparativ cu AlaGly libera, poate fi datorată următorilor factori:
- Împiedicarea schimbului dintre HDO și situsurile HN.
- Relaxarea accelerată a protonilor peptidei în prezenta LUVs prin dinamica de legare încetinită.
A fost observat un efect specific situsului, adică o reducere a intensității semnalelor Ala-NH3 în comparație cu cele ale Gly-HN (Tabelul 1, coloana III). Îmbunătățirea semnalului corelării Ala-HN/Ala-Hα a fost redusă de 14 ori, în timp ce corelarea Gly-HN/Ala-Hα a fost redusa doar cu un factor de 6.
Transferul hiperpolarizării de la HDO la amidele detectate se bazează pe: (i) schimbul chimic de protoni; (ii) schimb magnetic direct, adică NOE, de la solvent la protonii HN; (iii) schimb NOE retransmis. Experimentele 1D „water-selective” și 2D NOESY arată că transferul polarizării se bazează atât pe efectul NOE de la solvent cât și pe schimbul chimic (Figura 4).

Figura 4. (adaptat pentru materialul suplimentar a lucrarii noastre Sadet et al., JACS 2019)
a) Secvența de puls utilizată pentru „Selectiv Water-NOESY”; b) Experimente 1D NOE selectiv plecând de la magnetizarea apei. Transferul total de magnetizare către situsurile HN și alifatice atinge un maxim pentru timpul de transfer TM aproximativ 5 s. c) Spectru 2D 1H-1H NOESY al AlaGly înregistrat cu mixing time de 300 ms. Semnalele pozitive sunt ilustrate cu verde, iar cele negative cu roșu.
Chiar și peptidele de dimensiuni mici au proprietăți structurale diferite. Aceste structuri diferite sunt mai pronunțate în prezența partenerilor datorită interacțiunii. Peptidele amfifile formate din aminoacizi se leagă de veziculele lipidice prin reacții exoterme cu energii libere de legare, ΔG, care depind de secvența peptidei și variază între -10 și -80 kJ/mol. Lacunele energetice la acest ordin de magnitudine sunt tipice pentru partenerii puternic asociați. Creșterea dispersiei spectrale observată la adăugarea de lipozomi (Figura 3B) indică o împrăștiere în conformațiile peptidice. Această împrăștiere are loc la peste cca. 0.5 ppm, adică 400 Hz în condițiile noastre experimentale. Conformațiile majoritare care apar după introducerea lipozomilor generează semnale cu intensități similare. Scădere energiei de separare a acestor conformații la temperatura de studiu, T = 300K, este de ordinul ΔG ≈ −RT = −2.5 kJ/mol, unde R = 8.3 J K −1 mol −1 (constanta universală a gazelor). Pentru validarea modelului de interacțiune obținut în urma experimentelor, a fost folosită simularea „molecular dynamics” (MD). Peptida care interacționează cu lipida bistratificată a fost testată pentru 200 ns utilizând platforma de simulare „CHARMM”. Pentru peptida, pentru care s-a propus inițial o conformație aleatorie, s-a observat că aceasta stă un timp semnificativ în contact strâns cu suprafața bistratificată. Majoritatea legăturilor de hidrogen (92%) au apărut atunci când peptida a fost orientată cu reziduul Ala spre suprafața bistratificată (Figura 3D), legăturile de hidrogen formându-se între Ala N-terminal și fosfatidilcolină. Aceste lucruri arată că peptida cu sarcină pozitivă la N-terminal formează situsul primar de interacțiune cu suprafața membranei. Energiile de legare calculate cu MD, cuprinse în intervalul -0.98 – 12.89 kJ/mol, se potrivesc cu valoarea experimentală.
În concluzie, informațiile structurale pot fi obținute într-un minut prin spectroscopie 2D de corelație utilizând protoni hiperpolarizați HDO. Detectarea interacțiunilor bimoleculare, fără a recurge la îmbogățirea izotopică, face posibilă dezvoltarea de aplicații rapide și simple, cum ar fi screening-ul de droguri prin definirea legăturilor situsurilor biomoleculare utilizând spectroscopia de corelație hiperpolarizată.
Rezultatele experimentale obținute în aceasta etapă au fost diseminate prin publicare unui articol în Journal of the American Chemical Society (FI = 14.695).
Aude Sadet, Cristina Stavarache, Mihaela Bacalum, Mihai Radu, Geoffrey Bodenhausen, Dennis Kurzbach, Paul R. Vasos, „Hyperpolarized Water Enhances Two-Dimensional Proton NMR Correlations: A New Approach for Molecular Interactions”, Journal of the American Chemical Society, 2019, 141, 12448-12452, DOI: 10.1021/jacs.9b03651.
De asemenea, rezultatele obținute au fost diseminate print-o prezentare orală în cadrul unei manifestări științifice de către membrii echipei de cercetare:
Aude Sadet, Cristina Stavarache, Mihaela Bacalum, Mihai Radu, Geoffrey Bodenhausen, Dennis Kurzbach, Paul R. Vasos, „Water-Exchanging Hydrogens’ Positions in Biomolecules Detected via Long-Lived Coherences and Hyperpolarized 2D COSY”, 60th Experimental Nuclear Magnetic Resonance Conference, Oral presentation, April 7 – 12, 2019, Asilomar Conference Center in Pacific Grove, California, USA.
5. Rezultatele finale ale proiectului
Concluzii generale
In perioada august 2017 – noiembrie 2019 au fost publicate 5 articole ISI. Doua capitole de carte sunt in curs de publicare. Un brevet a fost depus la OSIM. Dintre articolele deja publicate, 2 articole sunt situate în zona maxima de influenta conform clasării UEFICSDI în domeniul chimie fizica.
- Cristina Stavarache, Anamaria Hanganu, Anca Paun, Codruta Paraschivescu, Mihaela Matache, Paul R. Vasos, “Long-lived states detect interactions between small molecules and diamagnetic metal ions”, Journal of Magnetic Resonance, 2017, 284, 15-19, http://dx.doi.org/10.1016/j.jmr.2017.09.001.
- Viorel Vasile Nastasa, Cristina Stavarache, Anamaria Hanganu, Adina Coroaba, Alina Nicolescu, Calin Deleanu, Aude Sadet, Paul Vasos, “Hyperpolarised NMR to Follow Water Proton Transport through Membrane Channels via Exchange with Biomolecules”, Faraday Discussions, 2018, 209, 67-82, DOI: 10.1039/C8FD00021B
- Manda, Hinescu, Neagoe, Ferreira, Boscenco, Vasos, Basaga, Cuadrado, Emerging Therapeutic Targets in Oncologic Photodynamic Therapy, Current Pharmaceutical Design, 24, 44, 5268-5295, 2018, doi: 10.2174/1381612825666190122163832
- Asavei, Bobeica, Nastasa, Manda, Naftanaila, Bratu, Mischianu, Cernaianu, Ghenuche, Savu, Stutman, Tanaka, Radu, Doria, Vasos, Medical Physics, 2019, 46 (10), 726-734, doi: 10.1002/mp.13741
- Aude Sadet, Cristina Stavarache, Mihaela Bacalum, Mihai Radu, Geoffrey Bodenhausen, Dennis Kurzbach, Paul R. Vasos, „Hyperpolarized Water Enhances Two-Dimensional Proton NMR Correlations: A New Approach for Molecular Interactions”, Journal of the American Chemical Society, 2019, 141, 12448-12452, DOI: 10.1021/jacs.9b03651.
- Aude Sadet, Cristina Stavarache, Florin Teleanu, Paul R. Vasos, “Water hydrogen uptake in biomolecules detected via nuclear magnetic phosphorescence”, Scientific Report, 2019, 9, 17118, https://doi.org/10.1038/s41598-019-53558-8.
Rezultatele obținute au fost diseminate prin prezentări în cadrul următoarelor manifestări științifice de către membrii echipei de cercetare:
- Paul Vasos, “Enhanced NMR to follow enzymatic reactions in living cells”, invited oral presentation, 20th Romanian International Conference on Chemistry and Chemical Engineering, 6-9 September 2017, Poiana Brasov, Romania.
- Aude Sadet, Cancer Research Institute, University of Cambridge, invited seminar, 6-9 December 2017, “Molecular probes useful for in vivo MRI experiments“.
- Aude Sadet, “Hyperpolarised NMR to Follow Water Proton Transport through Membrane Channels via Exchange with Biomolecules”, UK Royal Society, oral presentation, Faraday Discussions Meeting, Glasgow, June 2018.
- Aude Sadet, Cristina Stavarache, Mihaela Bacalum, Mihai Radu, Geoffrey Bodenhausen, Dennis Kurzbach, Paul R. Vasos, „Water-Exchanging Hydrogens’ Positions in Biomolecules Detected via Long-Lived Coherences and Hyperpolarized 2D COSY”, 60th Experimental Nuclear Magnetic Resonance Conference, Oral presentation, April 7 – 12, 2019, Asilomar Conference Center in Pacific Grove, California, USA.